偶然想到这个问题,我猜女儿再长大点一定会问。现在先暂停想一想,如果是你,会怎么回答?

认真思考,严肃回答,不许抖机灵拿出这种东西。
这个长篇答案,可能要女儿到中学了才能拿出来用。如果现在就问起来,我也许只能回答:“因为水把东西变冷了,火就烧不下去了。”
但是没关系,因为想知道答案的是我,所以可以继续深究下去。
火是如何存在的
要理解灭火,先要理解火。

中学化学告诉我们,燃烧需要三个要素,构成一个“燃烧三角”:
- 可燃物:能烧的东西,比如木头、汽油,这些本质上是还原剂。
- 助燃物:帮助燃烧的东西,通常是空气中的氧气,这些是氧化剂。
- 引火源:提供最初能量的东西,比如火柴的热量。
三者缺一不可。
顺带一提,助燃物不只有氧气。氢气也可以在氯气中燃烧,许多物质都能在氟气中剧烈燃烧。只是在地球上,氧气是最常见的助燃物。
这个思路很科学:水能灭火,一定是破坏了燃烧三要素中的至少一个。是哪一个?答案先捂着,继续深入。
现在,我们进入化学的微观世界,看看这三个要素是如何“烧起来”的。
这里有个不为人知的事实:液体本身并不燃烧。我们所见的绝大多数燃烧,其主战场都在气体中。
燃烧在微观层面来看,是可燃物的分子和助燃物的分子高速、有效地碰撞,发生剧烈的氧化还原反应,变成其他分子,并放出光和热。要实现高效碰撞,最好的形态就是气体,因为它们充分混合在一起了。你中有我,我中有你。
用一杯汽油做个思想实验。把它放进一个特别的装置,既是冰柜也是烤炉,从接近绝对零度(宇宙最低温)缓慢加热,而且不使用明火:
- 当温度达到约零下40℃时,汽油分子就开始获得足够能量,从液体表面挥发成气体。汽油蒸气向空气中扩散,离液面近浓度高,反之则低。有这层薄薄的蒸汽在,在上面快速打出一个火星,它就能把汽油蒸气“噗”地一次性烧掉,然后火焰熄灭。这个零下40℃,就是汽油的闪点,从这个温度开始,汽油可以点着火。
- 继续加热。当温度达到约280℃时,惊人的一幕发生了:即使没有火源,不打火星,汽油自己就猛地一下燃烧起来了,直到全部烧完才灭。这个温度,叫燃点。在燃点的温度,汽油蒸气分子与氧气分子碰撞非常剧烈,汽油分子每碰掉一个,发出的热还能从杯里再蒸发出一个。

发现没?火焰能持续下去的秘诀,是蒸发速度。越热蒸发越快,在燃点温度下,产生蒸气的速度,达到并超过了燃烧消耗的速度。这条燃料补给线一旦建立,燃烧就形成了正反馈,停不下来了。
固体燃烧的特殊性
固体燃烧比液体更复杂。我们用木柴燃烧来做另一个思想实验。
木柴燃烧分两个阶段:
第1阶段:有焰燃烧。
当木柴被点燃,它内部复杂的有机物大分子会分解,这个过程叫热解。热解产生了两种东西:可燃性气体(比如甲烷、一氧化碳)和固态的木炭(接近于碳单质)。

这个过程和液体燃烧很像,只是“蒸发”变成了“热解”。蒸发是物理变化,分子本身没变;热解是化学变化,大分子断裂成了小分子气体。这些可燃气体与空气混合后燃烧,就在木材的周围包了一圈漂亮的火焰。由于受热的气体总是往上跑,所以火焰总是出现在木柴顶端。
第2阶段:无焰灼烧。
当气体烧得差不多了,火焰消失,剩下红彤彤的木炭。此时,有焰燃烧结束了,进入了无焰的灼烧阶段。

这个过程更像冷兵器时代两军交锋。氧气分子是进攻方,直接冲到木炭的固体表面,与表面的碳原子厮杀。反应的产物二氧化碳是气体,它会立刻飞走。下方的、新鲜的碳原子补上锋线。这个过程周而复-复始,直到木炭消耗殆尽。至于灰烬,则是木炭中的一些非碳元素杂质。

木炭这种纯粹的表面燃烧,有一个巨大的优点:稳定可控。
它的放热速率,主要只取决于两个变量:可燃物的表面积和助燃物的供应量。表面积几乎不变,唯一的变量就是氧气量。因此,它的热量输出可以被精确控制,这使它成为一种非常理想的燃料,不仅仅因为热值高。

这种特性有其特殊用途。比如蒸汽火车,锅炉里烧的是煤炭(与木炭类似)。司炉可以通过控制风门 的开度,来调节进入炉膛的空气量,从而精确控制燃烧的剧烈程度,进而控制蒸汽的产生和火车的动力。
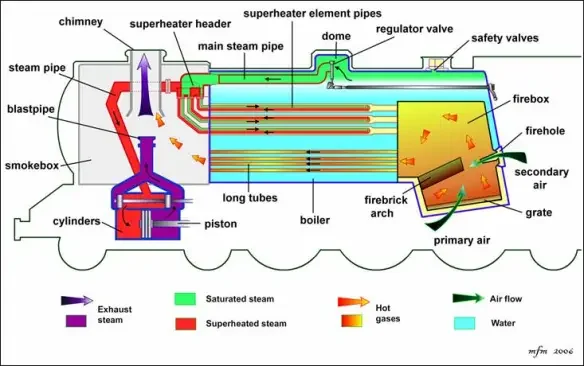
紫色箭头是废气排出,把橙黄色箭头热气从炉膛里抽过来,炉膛吸进绿色箭头空气。
比风门更巧妙的,是火车烟囱里的喷管,它会将驱动活塞后的废蒸汽高速排入烟囱,利用高速气流产生的负压,将新鲜空气更猛烈地吸入炉膛。这个原理是伯努利方程,流体(气体或液体)流速越快,压力越小,它周围的气体或液体,就会因为这边是压力小的“软柿子”向这边挤过来。喷管越喷,抽风约猛,炉膛里进氧气越快,火烧得越旺,产生更多蒸气。这是一个绝妙的正反馈循环。
那么,如果可燃物和助燃物都是固体呢?有这样的燃烧吗?

有,最典型的就是铝热反应。把铝粉(可燃物)和氧化铁粉(助燃物)混合,用高温点燃。铝会直接从氧化铁那里夺取氧原子,这个固-固反应释放的温度高达2500℃,足以把生成的铁熔化成液体。液态铁的存在,让粉末流动起来,极大地促进了两种分子的持续接触,使反应得以继续下去。
再极端一点,如果不提供助燃物,只对固态可燃物强力加热会怎样?
它只会热解,而不会燃烧。这是现代化工的重要一环。比如将煤隔绝空气加热(干馏),就能得到三种重要的工业原料:焦炭(用于炼钢)、煤焦油(化工原料)和煤气(燃料)。
现在回到一个根本问题:为什么木炭能有这种纯粹的表面燃烧方式,而液体燃料没有?这源于物质在分子层面的本质不同。

气体分子,像游泳池里的一堆玩具鸭,随机飘荡,自由碰撞。

液体分子,像一堆巴克球,被微弱的力聚在一起,但可以相互滑动。这点力很容易被热量克服,使它们“蒸发”,四散逃离。

固体分子(如碳),则像一座榫卯结构的建筑。每个原子都被强大的化学键锁死在原地。燃烧的热量远不足以拆散这个结构,原子无法逃逸成气体,只能留在原地,进行表面反应。比如碳的燃点就几百度,而升华点(气化温度)则高达3600度,真有那个气化温度,早就烧光了。
燃烧的本质
现在,有没有发现“燃烧三要素”这个说法有点可疑,似乎太笼统了。短暂燃烧和持续燃烧的条件并不相同。
- 短暂燃烧:需要可燃物、助燃物、达到蒸发/热解的温度、以及一个外部引火源。
- 持续燃烧:需要可燃物、助燃物、以及达到燃点的温度。
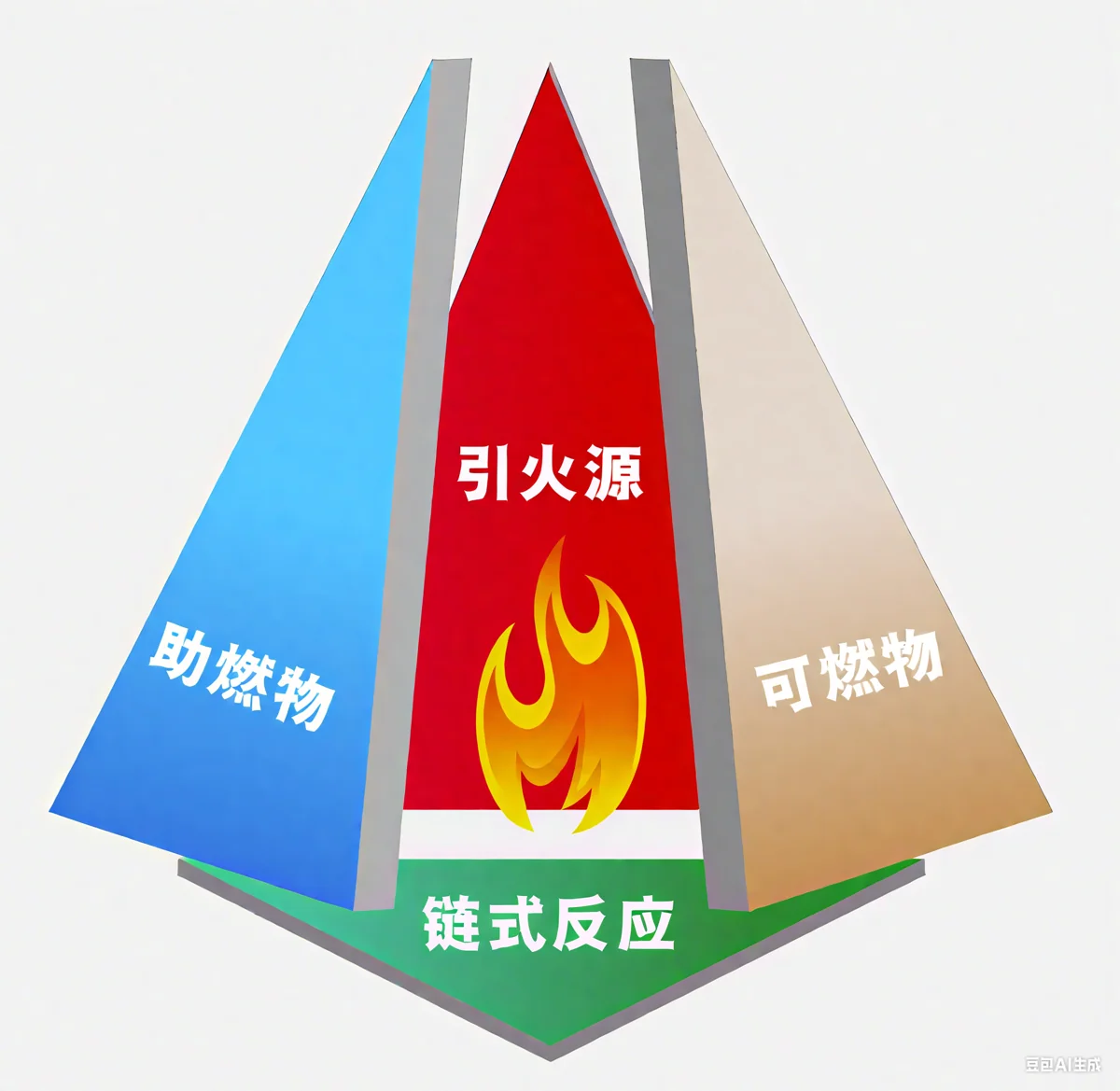
燃烧三角模型无法解释火焰为何能持续。于是科学家提出了“燃烧四面体”,增加了第四个因素:不受抑制的链式反应。
一旦燃烧开始,助燃剂分子与可燃物分子大量撞击,变成别的分子,放出热。但这还不是链式反应最厉害的地方。
除了完整分子相互碰撞,还有许多“碎片”分子参与反应。这些东西叫自由基,是在先前的剧烈碰撞中缺胳膊少腿的分子。有的电子被撞掉了一个,有的脸上糊着别人掉落的多余电子。自由基是饿狼,会疯狂攻击其他分子,试图恢复完整的状态。这反而加剧碰撞,产生更多热量和更多自由基。

这个过程像滚雪球一样自我复制、自我放大。这才是“火”最可怕也最伟大的地方。人类学会用火,力量不在于面对猛兽时一根火把的温度有多高。而在于这种四两拨千斤的力量,一把火可以把一片草原烤熟,捡完遍地食物还能垦成农田。这压倒了其他任何物种的身体力量。
另一个我们熟知的链式反应,是原子弹。

既然说到了原子弹,爆炸又是什么?是短暂燃烧还是持续燃烧?
(化学)爆炸通常归为短暂燃烧。环境温度达到闪点的情况下,空气中积累了足够多的气体可燃物,然后遇到一个局部温度达到燃点的引火源,引发了极快的链式反应。爆炸的积累阶段,环境温度会保持在燃点以下,否则还没等积累完成,自己就先烧完了。
答案揭晓
总结一下微观的燃烧过程:
- 气态可燃物:最直接,与助燃物混合即可燃烧。
- 液态可燃物:必须先蒸发成气体。
- 固态可燃物:大多需要先热解成气体(有焰燃烧),剩下的再进行表面燃烧(无焰灼烧)。
可以看到,除了少数特例,绝大多数燃烧都殊途同归,将战场转移到了气体中。
现在,我们终于可以回答最初的问题。水,到底是如何灭火的?它精准地攻击了“燃烧四面体”的哪个面:
- 攻击“热量”(冷却):这是水最主要的作用。水拥有极高的气化热,1克水变成水蒸气,需要吸收约2260焦耳的热量。要知道,这个能量大概可以把100斤的人提起来4米多高。当水泼向火时,它会疯狂吸热,热量蒸不出那么多气体可燃物了,链式反应中断。
- 攻击“助燃物”(窒息):相对次要多因素。水蒸发产生的巨量水蒸气,体积会膨胀上千倍。这些水蒸气驱赶走氧气,燃烧停止。
当然,并非所有火都能用水灭:
- 电器火灾:水能导电,可能导致触电或设备短路。
- 油类火灾:油比水轻,会浮在水面上,随水流淌,反而四下蔓延。
- 活泼金属火灾:如钾、钠、镁等,它们会与水发生化学反应,生成易燃的氢气,等于火上浇油。
说到底,水灭火最主要的原因,依然是它强大的冷却能力。这和开头的答案一样。
但有趣的是中间的探索过程。不假思索的答案,和历经探索得到的答案,其分量是完全不一样的。
要是我中学时能认识现在的自己,可能化学不至于不及格了。